การหาลำดับจีโนมของพืช/สัตว์เดอโนโว
ข้อดีของการบริการ
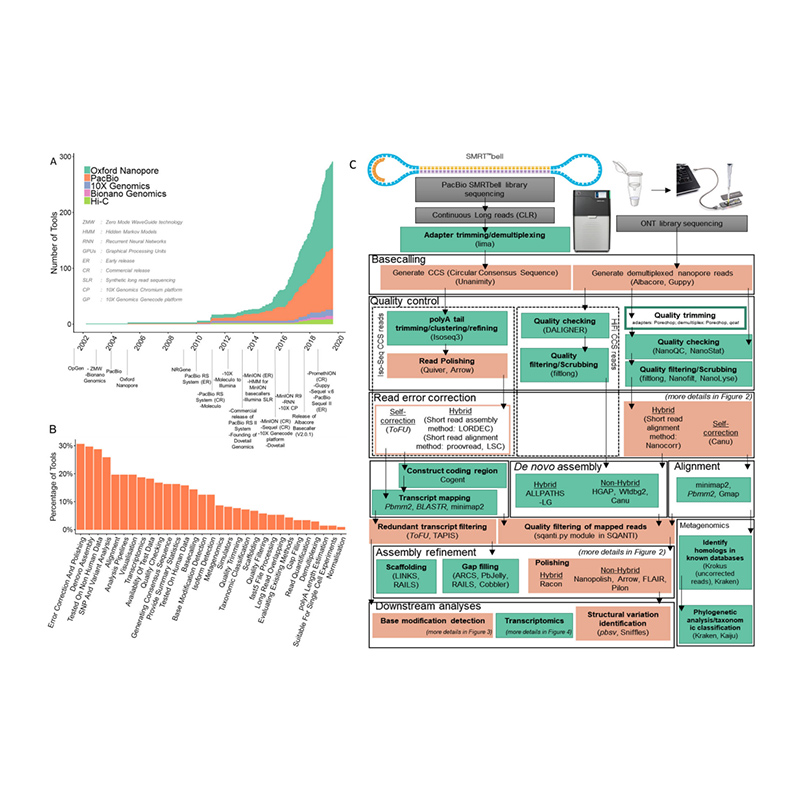
การพัฒนาแพลตฟอร์มลำดับและชีวสารสนเทศในเดโนโวการประกอบจีโนม
(Amarasinghe SL และคณะชีววิทยาจีโนม, 2563)
● การสร้างจีโนมใหม่และปรับปรุงจีโนมอ้างอิงที่มีอยู่สำหรับสายพันธุ์ที่สนใจ
● ความแม่นยำ ความต่อเนื่อง และความสมบูรณ์ในการประกอบที่สูงขึ้น
● การสร้างทรัพยากรพื้นฐานสำหรับการวิจัยเกี่ยวกับลำดับพหุมอร์ฟิซึม, QTL, การตัดต่อยีน, การผสมพันธุ์ ฯลฯ
● มาพร้อมกับแพลตฟอร์มการหาลำดับรุ่นที่สามอย่างเต็มรูปแบบ: โซลูชันการประกอบจีโนมแบบครบวงจรในที่เดียว
● กลยุทธ์การจัดลำดับและการประกอบที่ยืดหยุ่นเพื่อตอบสนองจีโนมที่หลากหลายพร้อมคุณสมบัติที่แตกต่างกัน
● ทีมนักชีวสารสนเทศที่มีทักษะสูงและมีประสบการณ์ที่ยอดเยี่ยมในการประกอบจีโนมที่ซับซ้อน รวมถึงโพลิพลอยด์ จีโนมขนาดยักษ์ ฯลฯ
● กรณีและปัญหาที่ประสบความสำเร็จมากกว่า 100 กรณี โดยมีปัจจัยผลกระทบที่เผยแพร่สะสมมากกว่า 900 กรณี
● ระยะเวลาดำเนินการเร็วถึง 3 เดือนสำหรับการประกอบจีโนมระดับโครโมโซม
● การสนับสนุนทางเทคนิคที่มั่นคงพร้อมชุดสิทธิบัตรและลิขสิทธิ์ซอฟต์แวร์ทั้งในด้านการทดลองและชีวสารสนเทศศาสตร์
ข้อมูลจำเพาะของบริการ
|
เนื้อหา
|
แพลตฟอร์ม
|
อ่านความยาว
|
ความคุ้มครอง
|
| การสำรวจจีโนม
| อิลลูมินา NovaSeq
| พีอี150
| ≥ 50X
|
| การจัดลำดับจีโนม
| PacBio รีวิโอ
| อ่านไฮไฟ 15 kb
| ≥ 30X
|
| ไฮ-ซี
| อิลลูมินา NovaSeq
| พีอี150
| ≥100X
|
ขั้นตอนการทำงาน

ข้อกำหนดตัวอย่างและการจัดส่ง
ข้อกำหนดตัวอย่าง:
| สายพันธุ์ | เนื้อเยื่อ | สำหรับแพคไบโอ | สำหรับนาโนพอร์ |
| สัตว์ | อวัยวะภายใน (ตับ ม้าม ฯลฯ) | ≥ 1.0 ก | ≥ 3.5 ก |
| กล้ามเนื้อ | ≥ 1.5 ก | ≥ 5.0 ก | |
| เลือดของสัตว์เลี้ยงลูกด้วยนม | ≥ 1.5 มล | ≥ 5.0 มล | |
| เลือดปลาหรือนก | ≥ 0.2 มล | ≥ 0.5 มล | |
| พืช | ใบสด | ≥ 1.5 ก | ≥ 5.0 ก |
| กลีบดอกหรือลำต้น | ≥ 3.5 ก | ≥ 10.0 ก | |
| รากหรือเมล็ด | ≥ 7.0 ก | ≥ 20.0 ก | |
| เซลล์ | การเพาะเลี้ยงเซลล์ | ≥ 3×107 | ≥ 1×108 |
การจัดส่งตัวอย่างที่แนะนำ
ภาชนะบรรจุ: หลอดหมุนเหวี่ยงขนาด 2 มล. (ไม่แนะนำให้ใช้ฟอยล์ดีบุก)
สำหรับตัวอย่างส่วนใหญ่ เราขอแนะนำไม่ให้เก็บรักษาในเอธานอล
การติดฉลากตัวอย่าง: ตัวอย่างจะต้องมีป้ายกำกับอย่างชัดเจนและเหมือนกับแบบฟอร์มข้อมูลตัวอย่างที่ส่งมา
การจัดส่ง: น้ำแข็งแห้ง: ตัวอย่างจะต้องบรรจุในถุงก่อนและฝังในน้ำแข็งแห้ง
ขั้นตอนการทำงานบริการ

การออกแบบการทดลอง
การจัดส่งตัวอย่าง
การสกัดดีเอ็นเอ
การก่อสร้างห้องสมุด
การเรียงลำดับ

การวิเคราะห์ข้อมูล
บริการหลังการขาย
*ผลการสาธิตที่แสดงไว้ที่นี่ทั้งหมดมาจากจีโนมที่เผยแพร่โดย Biomarker Technologies
1.Circos บนการประกอบจีโนมระดับโครโมโซมของกรัม. โรทันดิโฟเลียมโดยแพลตฟอร์มลำดับนาโนพอร์
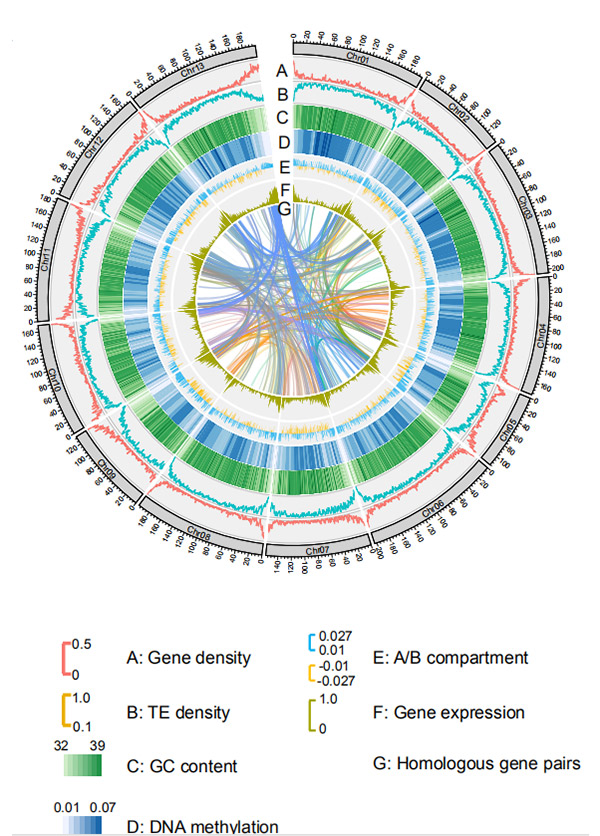
วังเอ็ม และคณะอณูชีววิทยาและวิวัฒนาการ, 2021
2. สถิติการประกอบจีโนมไรย์ของ Weining และคำอธิบายประกอบ
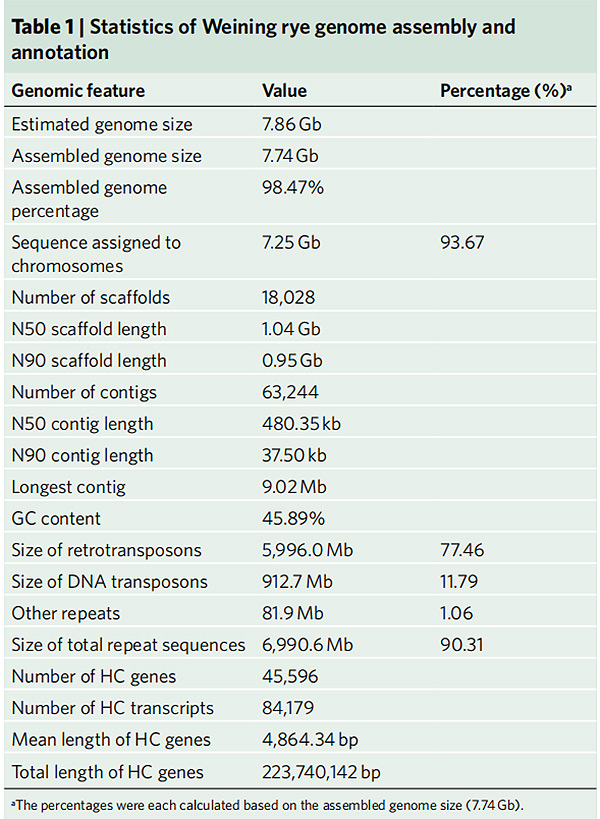
หลี่ จี และคณะพันธุศาสตร์ธรรมชาติ, 2021
3.การทำนายยีนของซีเชียม เอ็ดดูลจีโนมได้มาจากวิธีการทำนายสามวิธี:เดโนโวการทำนาย การทำนายตามความคล้ายคลึง และการทำนายตามข้อมูล RNA-Seq
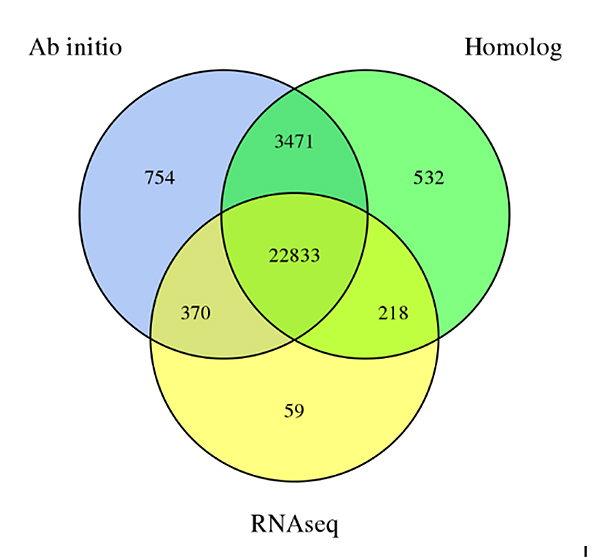
ฟูเอ และคณะการวิจัยพืชสวน, 2021
4.การระบุขั้วปลายยาวที่สมบูรณ์จะเกิดซ้ำในจีโนมฝ้าย 3 ชนิด
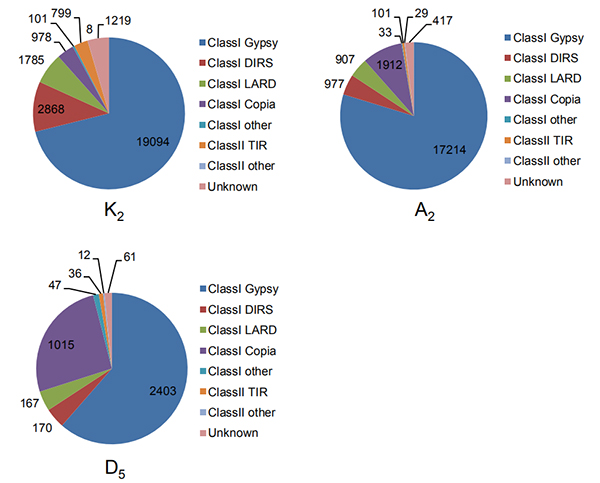
วังเอ็ม และคณะอณูชีววิทยาและวิวัฒนาการ, 2021
5.แผนที่ความร้อน Hi-C ของค. อะคูมินาตาจีโนมแสดงปฏิสัมพันธ์ทั่วทั้งจีโนมความเข้มของการโต้ตอบ Hi-C นั้นแปรผันตามระยะห่างเชิงเส้นระหว่างคอนติคเส้นตรงที่ชัดเจนบนแผนที่ความร้อนนี้บ่งชี้ถึงการยึดเกาะบนโครโมโซมที่มีความแม่นยำสูง(อัตราส่วนการยึดติด: 96.03%)
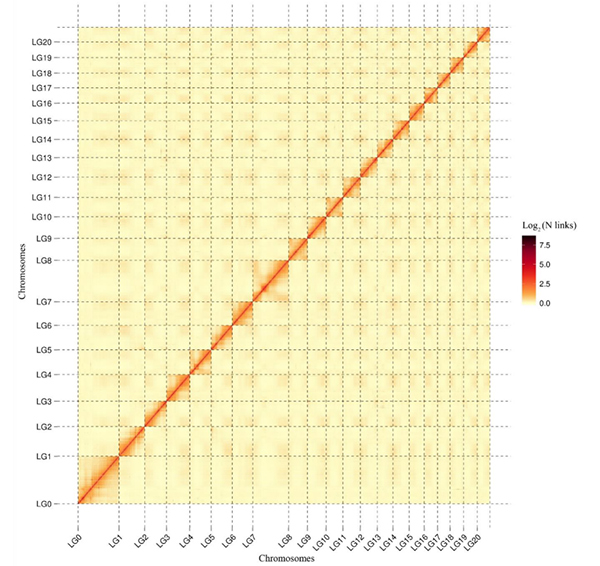
คัง เอ็ม และคณะการสื่อสารธรรมชาติ2021
คดีบีเอ็มเค
การประกอบจีโนมคุณภาพสูงเน้นย้ำคุณลักษณะจีโนมของไรย์และยีนที่สำคัญทางการเกษตร
ที่ตีพิมพ์: พันธุศาสตร์ธรรมชาติ, 2021
กลยุทธ์การจัดลำดับ:
การประกอบจีโนม: โหมด PacBio CLR พร้อมไลบรารี 20 kb (497 Gb, ประมาณ 63 ×)
การแก้ไขลำดับ: NGS พร้อมไลบรารี DNA 270 bp (430 Gb, ประมาณ 54 ×) บนแพลตฟอร์ม Illumina
การยึด Contigs: ไลบรารี Hi-C (560 Gb, ประมาณ 71 ×) บนแพลตฟอร์ม Illumina
แผนที่แบบออปติคอล: (779.55 Gb, ประมาณ 99×) บน Bionano Irys
ผลลัพธ์ที่สำคัญ
1. การประกอบจีโนมไรย์ของ Weining ได้รับการเผยแพร่โดยมีขนาดจีโนมรวม 7.74 Gb (98.74% ของขนาดจีโนมโดยประมาณโดยโฟลไซโตเมทรี)Scaffold N50 ของชุดประกอบนี้บรรลุผลสำเร็จ 1.04 Gb93.67% ของคอนติกถูกยึดไว้บนโครโมโซมเทียม 7 ตัวได้สำเร็จแอสเซมบลีนี้ได้รับการประเมินโดยแผนที่เชื่อมโยง LAI และ BUSCO ซึ่งส่งผลให้มีคะแนนสูงในการประเมินทั้งหมด
2.มีการศึกษาเพิ่มเติมเกี่ยวกับจีโนมเชิงเปรียบเทียบ แผนที่การเชื่อมโยงทางพันธุกรรม การศึกษาการถอดเสียงได้ดำเนินการบนฐานของจีโนมนี้มีการเปิดเผยลักษณะต่างๆ ที่เกี่ยวข้องกับคุณสมบัติจีโนม รวมถึงการทำสำเนาของยีนทั่วทั้งจีโนม และผลกระทบต่อยีนสังเคราะห์แป้งการจัดเรียงทางกายภาพของตำแหน่งโปรลามินที่ซับซ้อน การแสดงออกของยีนมีลักษณะการมุ่งหน้าในช่วงต้นและบริเวณโครโมโซมที่เกี่ยวข้องกับการเลี้ยงแบบสมมุติและตำแหน่งในไรย์
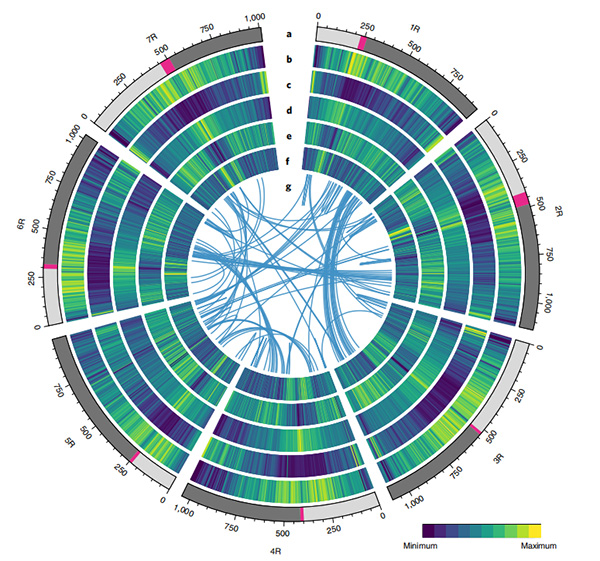 แผนภาพ Circos เกี่ยวกับคุณสมบัติจีโนมของจีโนมข้าวไรย์ของ Weining | 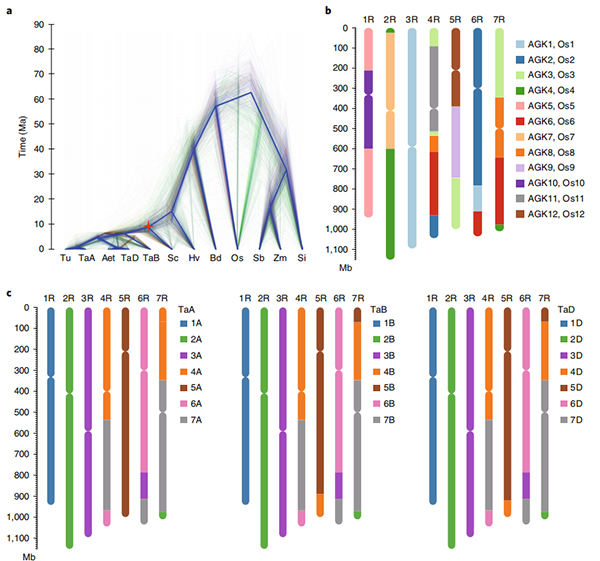 การวิเคราะห์เชิงวิวัฒนาการและโครโมโซมซินเทนีของจีโนมไรย์ |
Li, G. , Wang, L. , Yang, J.และคณะการประกอบจีโนมคุณภาพสูงเน้นย้ำคุณลักษณะจีโนมของไรย์และยีนที่สำคัญทางการเกษตรแนท เจเน็ต 53,574–584 (2021)
https://doi.org/10.1038/s41588-021-00808-z